The Telegraph Վերջերս հաղորդվել է, որ հանրությանը ասվել է, որ պետք է դադարեցնել հազի և մրսածության դեմ դեղամիջոցներ ընդունելը` կապված թմրամիջոցների, ֆոլկոդինի` ափիոնային հազի ճնշող դեղամիջոցի հետ կապված անվտանգության մտավախությունների պատճառով:
Հազի և մրսածության դեմ սովորական դեղամիջոցներից XNUMX-ը, այդ թվում՝ «Ցերեկային և գիշերային բուժքույր» պարկուճները, դեղերի կարգավորիչների հրամանով շտապ հանվել են շուկայից՝ անաֆիլաքսիայի՝ կյանքին սպառնացող անբարենպաստ դեպքի «շատ հազվադեպ» ռիսկի մտահոգության պատճառով:
«2-րդ դասի դեղերի հետկանչում» հայտարարությունը վերցված է Մեծ Բրիտանիայի կառավարության կողմից կայքը, ներկայացված է ստորև։

Երբ խոսքը վերաբերում է mRNA COVID-19 պատվաստանյութերին, կարգավորող երկակի ստանդարտները երբեք այդքան ակնհայտորեն ակնհայտ չեն եղել:
Անաֆիլաքսիան որպես կարևոր վտանգ ճանաչվել է Եվրոպական դեղամիջոցների գործակալության կողմից 2020 թվականի դեկտեմբերին EMA-ի CHMP-ում (Մարդկային օգտագործման համար նախատեսված դեղամիջոցների կոմիտե) գնահատման հաշվետվություն Pfizer-BioNTech COVID-19 պատվաստանյութի վրա՝ տես ստորև:
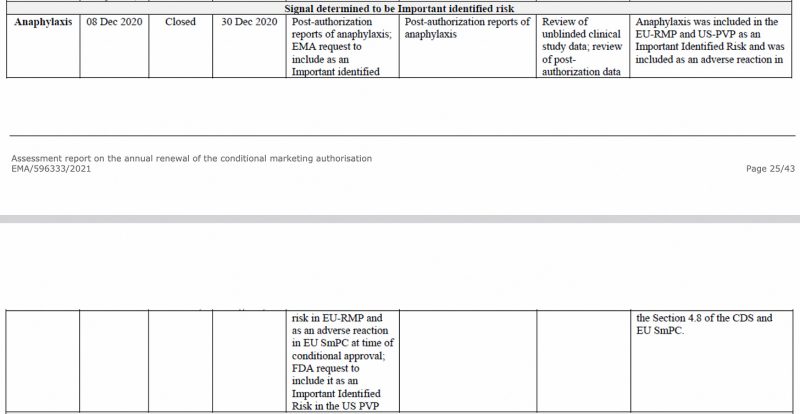
Նաև ԵՄ-ի Անվտանգության առաջին պարբերական թարմացումում հաշվետվություն, որը ես նախկինում ունեցել եմ վերլուծել, անաֆիլաքսիան կրկին նշվեց որպես կարևոր բացահայտված ռիսկ:

Դեղագործական զգոնության այս զեկույցում բացահայտվել է 3,827 համապատասխան դեպք (անհատ)՝ հետլիազորման տվյալներից։ Ամենաբարձր հիվանդացություն ունեցող երկիրը Ճապոնիան է, որին հաջորդում են ԱՄՆ-ը և Մեծ Բրիտանիան:
Ամենաշատ դեպքերը գրանցվել են կանանց շրջանում՝ ցնցող՝ 3,182 դեպք՝ տղամարդկանց 454 դեպքի համեմատ, միջին տարիքը՝ 44: Այն փաստը, որ կանանց մոտ 7 անգամ ավելի շատ դեպքեր են գրանցվել, նորություն չէ: Դեռևս 2021 թվականի դեկտեմբերին Ի վերլուծել Pfizer-ը պատրաստեց փաստաթուղթ FDA-ի համար, ընդգրկելով 3-ամսյա ժամանակահատվածը՝ 2020 թվականի դեկտեմբերից մինչև 28 թվականի փետրվարի 2021-ը, անաֆիլաքսիսի դեպքում կանայք 8 անգամ ավելի շատ են տուժել:
Այսպիսով, համապատասխան անբարենպաստ իրադարձությունների 98 տոկոսը (ներառյալ անաֆիլակտիկ ռեակցիան, անաֆիլակտիկ շոկը, անաֆիլակտոիդ ռեակցիան և անաֆիլակտոիդ շոկը) դասակարգվել են որպես լուրջ:
Ավելին, դեպքերի 92 տոկոսի համար պատվաստանյութի ընդունումից հետո անբարենպաստ դեպքի առաջացման ժամանակն անցել է 24 ժամից պակաս:

Ճակատագրական արդյունքներ
3,922 իրադարձություններից 28-ը մահացու էին, իսկ ապշեցուցիչ 704-ի համար արդյունքն անհայտ էր: Մահացու ելքի դեպքերի համարներ չեն նշվում։

Դեպքեր ըստ տարիքային խմբի
Համապատասխան 3,827 դեպքից (անհատ) 23-ը եղել են մանկական տարիքային խմբից, իսկ 3,021-ը` մեծահասակների տարիքային խմբից:
Համակցված հիվանդությունների առկայություն
Հատկանշականն այն է, որ անաֆիլաքսիայի դեպքերի մոտավորապես 2/3-ը եղել է Նշում ունեք որևէ ուղեկցող հիվանդություն (առողջական խնդիրներ):

Հաշվի առնելով այն, ինչ տեղի է ունեցել mRNA COVID-19 պատվաստանյութերի շրջանառությունից հետո, զարմանալի չէ կարդալ.անվտանգության նոր տեղեկություններ չեն հայտնաբերվել կապված BNT162b2-ով անաֆիլաքսիայի ռիսկի հետ» (Pfizer-BioNTech COVID-19 պատվաստանյութ): Բերված պատճառն (կամ նրանց թաքնված արդարացումն այն է, որ «այդ ռիսկը հաղորդվում է.. որը ներառում է համապատասխան գործողությունների մասին տեղեկատվություն, որոնք պետք է ձեռնարկվեն հետևյալ կերպ. Պատվաստանյութի ընդունումից հետո հազվադեպ անաֆիլակտիկ իրադարձության դեպքում»։
Under Կանոնակարգ 174, Տեղեկություններ Մեծ Բրիտանիայի առողջապահության մասնագետների համար, որը վերջին անգամ վերանայվել է 2021 թվականի դեկտեմբերին, ասվում է հետևյալը.

n փաստորեն, հենց ԱռԱջին օր Միացյալ Թագավորությունում Pfizer-BioNTech COVID-19 պատվաստանյութի տարածման ժամանակ գրանցվել է անաֆիլաքսիայի երկու դեպք և հնարավոր ալերգիկ ռեակցիայի մեկ դեպք: Սա չխանգարեց MHRA-ին հետ կանչել արտադրանքը. նրանք պարզապես շրջանցեցին խնդիրը՝ հայտարարելով, որ մարդիկ, ովքեր ունեն ալերգիայի պատմություն, չպետք է պատվաստանյութ ընդունեն:
Նույնիսկ այն ժամանակ, երբ նրանք գիտեին,- Pfizer/BioNTech-ի լիպիդային նանոմասնիկների բաղադրիչները ALC-0159 և ALC-0315 նախկինում երբեք չեն ներառվել որևէ լիցենզավորված դեղամիջոցի մեջ: ALC-0159-ը պարունակում է PEG (պոլիէթիլեն գլիկոլ), որը հայտնի է, որ առաջացնում է անաֆիլաքսիա.
Դա միանշանակ է. անաֆիլաքսիան հայտնի էր կյանքին սպառնացող անբարենպաստ իրադարձություն, մոտավորապես նույն ժամանակ, երբ շտապ օգտագործման թույլտվություն տրվեց Pfizer-BioNTech COVID-19 պատվաստանյութի համար: Այնուամենայնիվ, քանի որ դա «ներարկվող պատվաստանյութ» է, այն ինչ-որ կերպ ստացել է անվճար անցում դեղերի բոլոր կարգավորող մարմիններից, անկախ նրանից, թե որքան սարսափելի տվյալներ են կուտակվում, երբ հազի օշարակը կամ պարկուճը, մյուս կողմից, շտապ հետ է կանչվում՝ հիմնվելով «ա Անաֆիլաքսիայի շատ հազվադեպ ռիսկ»:
Վերահրատարակվել է հեղինակայինից Ենթարկ
Հրատարակված է Ա Creative Commons Attribution 4.0 միջազգային լիցենզիա
Վերատպումների համար խնդրում ենք կանոնական հղումը վերադարձնել բնօրինակին Բրաունսթոունի ինստիտուտ Հոդված և հեղինակ.









