Այս շաբաթ ԱՄՆ Սննդի և դեղերի վարչությունը (FDA) լիազորված Pfizer-ի Covid-19 պատվաստանյութի մեկ խթանիչի օգտագործումը 5-11 տարեկան երեխաների մոտ՝ պատվաստումների առաջնային շարքի ավարտից առնվազն հինգ ամիս հետո։ Սպասվում է, որ CDC-ի խորհրդատվական կոմիտեն այսօր կկնքի որոշումը:
Ըստ FDA-ի, իր որոշման հիմքում ընկած ապացույցները եկել են 67 երեխաների ենթաբազմությունից, ովքեր մասնակցել են ընթացիկ փորձարկմանը և ուժեղացվել են իրենց հիմնական շարքից 7-9 ամիս անց: Նրանք ցույց են տվել հակամարմինների ավելի բարձր մակարդակներ՝ խթանիչից մեկ ամիս անց, համեմատած խթանիչից առաջ:
FDA-ի որոշումը համարձակ է մի քանի պատճառներով.
Տվյալների բացակայություն
Հենց այն ժամանակ, երբ FDA-ն պետք է ավելի լավ տվյալներ պահանջի, գործակալությունը իջեցնում է իր չափանիշները:
Այս տարիքային խմբում ոչ մի խիստ ուսումնասիրություն ցույց չի տվել, որ երրորդ դեղաչափը կարող է նվազեցնել այնպիսի կարևոր արդյունքներ, ինչպիսիք են հոսպիտալացումները և մահերը. պատահական կլինիկական փորձարկումները չեն իրականացվել, չնայած Pfizer-ը միլիարդավոր եկամուտներ է ստանում:
Փոխարենը, որոշումը հիմնված էր «չեզոքացնող հակամարմինների» առկայության վրա, քանի որ դրանք հեշտ է չափել և ուսումնասիրել: Հակամարմինների մակարդակը ոչ միայն արագ է մարում, այլև պարտադիր չէ, որ դրանք կապված լինեն պաշտպանության հետ:
FDA-ի սեփական կայքը ասում է, որ «հակամարմինների թեստերը չպետք է օգտագործվեն մարդու իմունիտետի մակարդակը կամ Covid-19-ից պաշտպանվածությունը գնահատելու համար»։ Եվ այնուամենայնիվ, սա այն է, ինչ արել է գործակալությունը։
Սա հետևում է նախորդին տվյալներ Նյու Յորքից Omicron աճի ժամանակ, որը ցույց է տալիս Pfizer-ի պատվաստանյութի արդյունավետությունը 5-11 տարեկան երեխաների մոտ 68%-ից իջել է 2021թ.-ի դեկտեմբերի կեսերին՝ մինչև 12թ.
Դեղորայքի կարգավորիչների և առողջապահական մարմինների կողմից հակամարմինների վրա կարճատեսորեն ուշադրություն դարձնելը եղել է իմունային համակարգի այլ կարևոր ասպեկտների հաշվին, ինչպիսիք են CD4+ T-բջիջները և բնական մարդասպանների պատասխանները, որոնք վճռորոշ դեր են խաղում վարակի կանխարգելման գործում և համարվում են ավելի դիմացկուն, քան հակամարմինները: Ցավոք, այս տվյալները հիմնականում անտեսվել են իշխանությունների կողմից:
FDA-ի Կենսաբանական գնահատման և հետազոտությունների կենտրոնի տնօրեն դոկտոր Փիթեր Մարքսը խոստովանեց, որ. տվյալները գնալով ցույց են տալիս այդ պաշտպանությունը երկու չափաբաժիններից հետո թուլանում է ժամանակի ընթացքում, և որ երրորդ ներարկումը կարող է նպաստել 5-ից 11 տարիքային խմբի երեխաների պաշտպանությանը, քանի որ «օգուտները գերազանցում են ռիսկերը»:
Այնուամենայնիվ, անվտանգության առումով, FDA-ն գնահատել է միայն մոտավորապես 400 երեխայի, ովքեր ստացել են խթանող դոզան, և որևէ լուրջ, հազվագյուտ վնաս չի հայտնաբերվի նման փոքր նմուշի չափով:
Անտեսելով բնական անձեռնմխելիությունը
Երրորդ չափաբաժինը թույլ տալով բոլոր 5-11 տարեկան երեխաների համար, որոնց մեծ մասն արդեն բնական իմունիտետ ունի, դժվար թե հետագա օգուտներ բերի և կարող է նրանց ենթարկել անհարկի վնասի:
ԱՄՆ CDC մասին որ երեխաների և դեռահասների մոտ 75%-ն ունի շճաբանական ապացույցներ (հակամարմիններ) նախորդ վարակի հետևանքով և, հետևաբար, արդեն մշակել է ամուր և ամուր պաշտպանություն COVID-19-ից։
Մեծ Բրիտանիայի կառավարությունը գնահատվում որ 85-5 տարեկան երեխաների ավելի քան 11%-ը վարակվել է Covid-19-ով մինչև 2022թ.
Մարտի Մակարի, Ջոնս Հոփկինսի բժշկական դպրոցի պրոֆեսոր գրել The Wall Street Journal-ում նշվում է, որ բնական անձեռնմխելիությունը, ամենայն հավանականությամբ, շատ ամուր կլինի երեխաների մոտ՝ հաշվի առնելով նրանց ավելի ուժեղ իմունային համակարգը: Նա ասաց, որ եթե երեխան արդեն ունեցել է Covid-19, «պատվաստման համար գիտական հիմք չի լինի»:
Նա նաև նկատեց, որ Covid-19-ի ոչ մի դեպք չի արձանագրվել ոչ պատվաստված խմբում, ոչ էլ պլացեբո խմբում երեխաների մոտ, որոնք նախկինում վարակվել են SARS-CoV-2-ով Pfizer-ի փորձարկման ընթացքում՝ ամրապնդելով բնական անձեռնմխելիության առավելությունները:
Խորհրդատվական վահանակ
Պատվաստանյութերի և հարակից կենսաբանական արտադրանքների խորհրդատվական կոմիտեն (VRBPAC) ոչ միայն պատկերացում և փորձաքննություն է տրամադրում գործակալությանը, այլև վստահություն և վստահություն է հաղորդում FDA-ի որոշումների կայացման գործընթացին:
Այնուամենայնիվ, FDA-ն այս շաբաթ չհրավիրեց իր խորհրդատվական խումբը՝ ասելով, որ այն արդեն քննարկել է խթանիչներին նախորդ հանդիպման ժամանակ, և որ հետագա քննարկումը ոչ մի օգուտ չի բերի:
Որոշ անդամներ մտահոգություն են հայտնել, որ դեղերի կարգավորիչը բազմիցս առաջ է շարժվել խթանող չափաբաժինների վերաբերյալ որոշումներով՝ առանց բաց հանրային քննարկումներ անցկացնելու, և ասում են, որ գործակալությունը ավելի ու ավելի քիչ է հույսը դնում իր անկախ փորձագետների վրա՝ նախքան դեղերը հաստատելը:
Է վերջին վերլուծությունըՀետազոտողները ցույց են տվել, որ FDA-ի կողմից հաստատված դեղերի միայն 6%-ն է վերանայվել խորհրդատվական խմբերի կողմից 2021 թվականին՝ 55-ի 2010%-ից ցածր (տես նկարը):
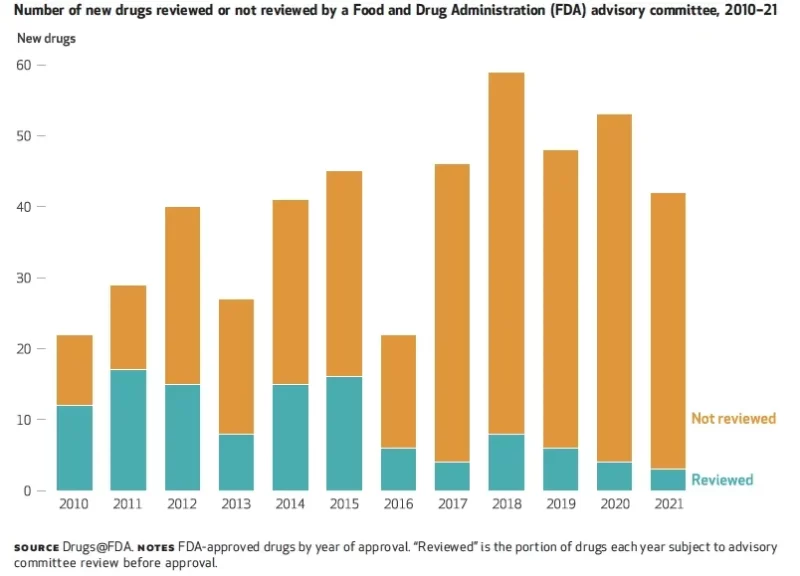
Եթե հանրային վստահությունն արտացոլում է այս թվերը, կարգավորող մարմինները երկար ճանապարհ ունեն անցնելու իրենց որոշումների կայացման գործընթացներում վստահությունը վերականգնելու համար:
Կլանո՞ւմ
Չնայած խթանիչների շարունակական ընդլայնմանը, պատվաստանյութերի հանդեպ ոգևորությունը կարծես թե նվազում է: Covid-19-ի պատվաստանյութերն այնքան արդյունավետ չեն վարակի և փոխանցման կանխարգելման համար, որքան ի սկզբանե ակնկալվում էր, և երեխաների մոտ լուրջ հիվանդության նման փոքր ռիսկի դեպքում ծնողները դառնում են ավելի քիչ համոզված:
A ԱՄՆ վերջին հարցումը պարզվել է, որ 5 տարեկանից ցածր երեխաների ծնողների գրեթե մեկ երրորդն ասել է, որ իրենք «միանշանակ չեն» պատվաստեն իրենց երեխային, ևս 11%-ը նշել է, որ դա կանի միայն անհրաժեշտության դեպքում (պարտադիր), իսկ 38%-ը ծրագրում է սպասել, որպեսզի կարգի բերի: տեսնել, թե ինչպես է պատվաստանյութն աշխատում ուրիշների համար:
Pfizer-ը դեռ պետք է իր դիմումը ներկայացնի FDA-ին 5 տարեկանից ցածր երեխաների համար երեք դոզայով պատվաստանյութի վերաբերյալ, սակայն ակնկալվում է, որ դա կանի առաջիկա շաբաթներին:
Սկզբնապես տեղադրվել է հեղինակի Կայքի
Հրատարակված է Ա Creative Commons Attribution 4.0 միջազգային լիցենզիա
Վերատպումների համար խնդրում ենք կանոնական հղումը վերադարձնել բնօրինակին Բրաունսթոունի ինստիտուտ Հոդված և հեղինակ.









